
fot. mario
Antybiotyki to jedne z najważniejszych leków, jakie mamy. Ale od dawna jest z nimi kłopot – nowych brak, a na stare bakterie się uodparniają. Na szczęście najnowsze odkrycia znowu dają nam szansę na skuteczną broń.
Choć o potrzebie odkrywania i wprowadzania na rynek nowych antybiotyków słyszymy od lat, a ich brak stanowi rzeczywisty problem, nadal trudno sobie wyobrazić, jak wyglądałoby nasze życie bez nich. Pokoleniu dzisiejszych 60 i 70-latków dzieciństwo upływało w „złotej erze” antybiotyków. Penicylina, odkryta w 1928 roku, dziesięć lat później była już masowo produkowana. W 1942 roku odkryto streptomycynę, która stała się pierwszym skutecznym lekiem przeciwko gruźlicy. Jak istotne były to odkrycia, świadczy fakt, że zarówno Alexander Fleming, jak i Selman Waksman zostali za nie uhonorowani Nagrodami Nobla.
W latach 40.-60. XX wieku dokonano odkrycia większości używanych dziś antybiotyków. W kolejnych latach obserwowano powolny spadek liczby odkrywanych nowych związków aktywnych. Za przykład niech posłużą dane Agencji Leków i Żywności (ang. Food and Drug Administration, FDA), która w latach 80. w ciągu połowy dekady (1983-87) zaaprobowała do użycia aż 16 nowych leków, podczas gdy w podobnym okresie na początku XXI wieku (2008-2013) – tylko dwa. Co więcej, w ostatnim ćwierćwieczu (od 1987 roku) nie odkryto żadnej nowej klasy antybiotyków.
Zgodnie z raportem Pew Research Center w maju 2015 roku w Stanach Zjednoczonych na różnych etapach badań klinicznych znajdowało się 36 związków, wśród których tylko 8 było w III fazie badań klinicznych, a dane historyczne wskazują, że jedynie 60% z nich ma szansę stać się lekami. Nic więc dziwnego, że naukowcy biją na alarm, szczególnie w świetle rosnącej antybiotykooporności. Tegoroczne doniesienia naukowe dają jednak podstawy ku temu, aby nieco bardziej optymistycznie spojrzeć w przyszłość. Co się zmieniło?
Nowe stare metody
W styczniu tego roku w czasopiśmie „Nature”[1] ukazała się praca opisująca nowo odkryty antybiotyk – teiksobaktynę (ang. teixobactin). Ten związek charakteryzuje się ciekawymi właściwościami: jego działanie opiera się na wiązaniu z lipidami (a nie białkami) odpowiedzialnymi za powstawanie ściany komórkowej bakterii; tworzy również nową klasę antybiotyków – inhibitorów syntezy peptydoglikanu. Najistotniejsza była jednak metodologia wykorzystana do jego odkrycia.
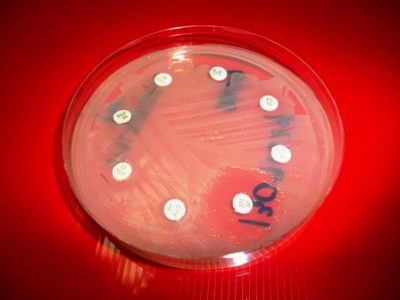
Badanie lekooporności Fot. Iqbal Osman
W złotych latach antybiotyków wykorzystywano metodę skriningu fenotypowego. Idea została zaczerpnięta z natury – bakterie wytwarzają związki, które zabijają inne mikroby. Naukowcy zatem przenosili bakterie do laboratorium, gdzie tworzyli „sztuczne ringi walki o życie”, obserwując inhibicję wzrostu bakterii pod wpływem czynników wytwarzanych przez inne gatunki. Metoda ta była bardzo wydajna i dzięki niej w latach 40., 50.-tych i 60.-tych XX wieku zidentyfikowano np. chloramfenikol czy cefalosporyny. Źródło potencjalnych nowych związków aktywnych szybko jednak wyschło. Okazało się bowiem, że nie potrafimy hodować w laboratorium bardzo dużej liczby bakterii. Naukowcy uświadomili sobie, że w naturze jest ogromna ilość nieodkrytych antybiotyków, których, w związku z trudnościami laboratoryjnymi, nie potrafią zidentyfikować.
Praca opublikowana w styczniu tego roku w „Nature” nie byłaby możliwa, gdyby badacze nie stworzyli nowego urządzenia, dającego możliwość pokonania problemu „niehodowalności laboratoryjnej” bakterii. Urządzenie o nazwie iChip zastępuje wysłużone szalki Petriego. Składa się ono z maleńkiej płytki agarowej otoczonej z dwóch stron półprzepuszczalnymi membranami, które umożliwiają przepływ składników odżywczych i czynników wzrostu. Próbkę gleby rozcieńcza się tak, aby do urządzenia dostała się pojedyncza komórka bakteryjna, która osiada na agarze. Następnie urządzenie umieszcza się w glebie w miejscu, z którego pobrano próbki, a w iChipie tworzy się kolonia bakteryjna, którą w kolejnym etapie znacznie łatwiej przenieść do hodowli laboratoryjnej. Dzięki tej technologii jesteśmy w stanie hodować około 50% bakterii występujących w glebie, podczas gdy wykorzystując standardowe hodowle laboratoryjne, można wyhodować jedynie około 1%. Opisanemu systemowi zawdzięczamy zidentyfikowanie teiksobaktyny, która wykazuje działanie przeciwko bakteriom Gram-dodatnim, a także szczepom antybiotykoopornym.
Nowe leki na stare cele
Do poszukiwań nowych leków naukowcy wykorzystują też inne wysłużone metody badawcze – na przykład działanie na określony, wcześniej ustalony cel gwarantujący sukces terapii. Najważniejszymi kryteriami przy identyfikacji potencjalnych antybiotyków są aktywność wobec bakterii i brak szkodliwego działania na organizmy zwierzęce. Już wiele lat temu badacze zorientowali się, że dobrym celem terapeutycznym będzie ściana komórkowa bakterii, ponieważ komórki ludzkie nie mają ściany komórkowej.
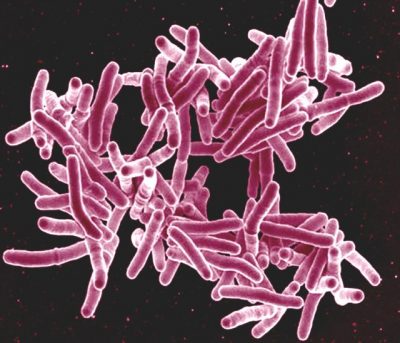
Prątki gruźlicy (Mycobacterium tuberculosis). Fot. NIAID
Niestety bakterie z biegiem czasu nabywają oporność na istniejące już antybiotyki. Przykładem może być prątek gruźlicy czyli Mycobacterium tuberculosis – bakteria, która stwarza realne zagrożenie dla życia ludzi, szczególnie w krajach rozwijających się. Uzyskała oporność na wiele antybiotyków, w tym jeden z podstawowych stosowanych w terapii gruźlicy, a działających właśnie na ścianę komórkową – Izoniazyd. Związek ten podawany jest w formie proleku i dopiero po aktywacji przez pewien enzym bakteryjny staje się lekiem aktywnym. W efekcie nabywania oporności na antybiotyki bakterie „nauczyły się” jednak wyłączać białko, które jest odpowiedzialne za przejście Izoniazydu z formy proleku do leku aktywnego. Naukowcom z firmy Novartis udało się niedawno znaleźć nowy lek przeciwgruźliczy[2], który działa na ten sam cel terapeutyczny co Izoniazyd, lecz nie wymaga wspomnianej aktywacji.
Nieznane możliwości
W jednym z ostatnich numerów czasopisma „Nature”[3] ukazała się praca, która łączy wszystkie dotychczas znane metody poszukiwania leków antybakteryjnych. Naukowcy z firmy Merck zastosowali skrining fenotypowy, lecz w bardziej wysublimowanej wersji. Skupili się tylko na obserwacji efektu, jaki analizowane substancje czynne wywierały na określony szlak metaboliczny – syntezę witaminy B2. Szlak ten jest aktywny tylko wtedy, gdy bakterie muszą same syntezować witaminę (nie mogą jej pobierać ze środowiska). Naukowcy założyli więc, że tylko związki, których działanie będzie zależne od obecności lub braku witaminy B2 w środowisku, będą potencjalnymi inhibitorami tego szlaku metabolicznego. Po przetestowaniu 57 tysięcy (!) cząsteczek zidentyfikowali związek o nazwie rybocyl (ang. ribocil), który spełniał zadane kryteria. Najciekawsze jednak było dopiero przed nimi. Okazało się, że związek nie działa na białka, ani nawet na lipidy (co już w pracy z wykorzystaniem iChipu było wielkim zaskoczeniem), a na niekodujący fragment bakteryjnego DNA. Oznacza to, że cząsteczka potrafi wpływać na regulację genów, a nie tylko na pojedynczy cel, np. białko. Po dokładniejszych badaniach ustalono, że w podobny sposób odbywa się włączanie i wyłączanie szlaku syntezy witaminy B2 w organizmie bakterii w zależności od dostępności witaminy. Nowy związek blokuje jednak transkrypcję genów odpowiedzialnych za syntezę witaminy nawet wtedy, gdy bakterie nie mogą jej pobrać ze środowiska, w ten sposób prowadząc do ich śmierci. Naukowcom udało się więc po raz kolejny podejrzeć i wykorzystać (chyba nie do końca świadomie) mechanizm obecny w naturze.
[1] Nature. 2015 Jan 22;517(7535):455-9. doi: 10.1038/nature14098 [2] Sci Transl Med. 2015 Jan 7;7(269):269ra3. doi: 10.1126/scitranslmed.3010597. [3] Nature. 2015 Oct 29;526(7575):672-7. doi: 10.1038/nature15542
dr Agnieszka Ludwig-Gałęzowska jest biologiem związanym z Uniwersytetem Jagiellońskim Collegium Medicum. W ramach pracy naukowej zajmuje się chorobami cywilizacyjnymi, w szczególności nowotworami i cukrzycą. Zaangażowana w popularyzację nauki – zarówno wśród dorosłych, jak i dzieci.



You must be logged in to post a comment.