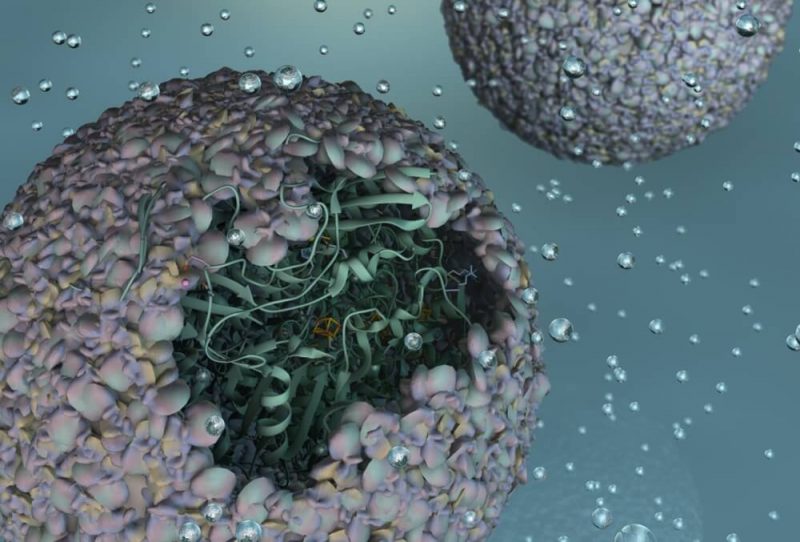
To może być klucz do czystego i taniego biopaliwa. Fot. Indiana University
Naukowcy z Uniwersytetu Indiana stworzyli wysoce wydajny biomateriał, który katalizuje formowanie się wodoru – jedną z połówek ostatecznego celu badaczy, jakim jest rozdzielenie H2O, aby wytworzyć wodór i tlen. Korzystając z tych pierwiastków, możliwy staje się tani i wydajny sposób zasilania samochodów, jeżdżących “niemal” na wodzie. Brzmi jak science fiction, prawda?
Zmodyfikowany enzym, biorący swe zalety z ochrony wewnątrz proteinowej skorupy – “kapsydu” – wirusa bakterii, posiada cechy, dzięki którym ten nowy materiał jest nawet 150 razy wydajniejszy w porównaniu do niezmienionej formy enzymu.
Według opisu całego procesu, opublikowanego w Nature Chemistry:
“Upraszczając, skorzystaliśmy z umiejętności wirusa do samodzielnej budowy szeregu bloków genetycznych i dodaliśmy do tego bardzo delikatny i wrażliwy enzym, który posiada niesamowitą właściwość wchłaniania protonów i wytwarzania wodoru,” powiedział przewodzący badaniu Trevor Douglas, Profesor Chemii Uniwersytetu Indiana.
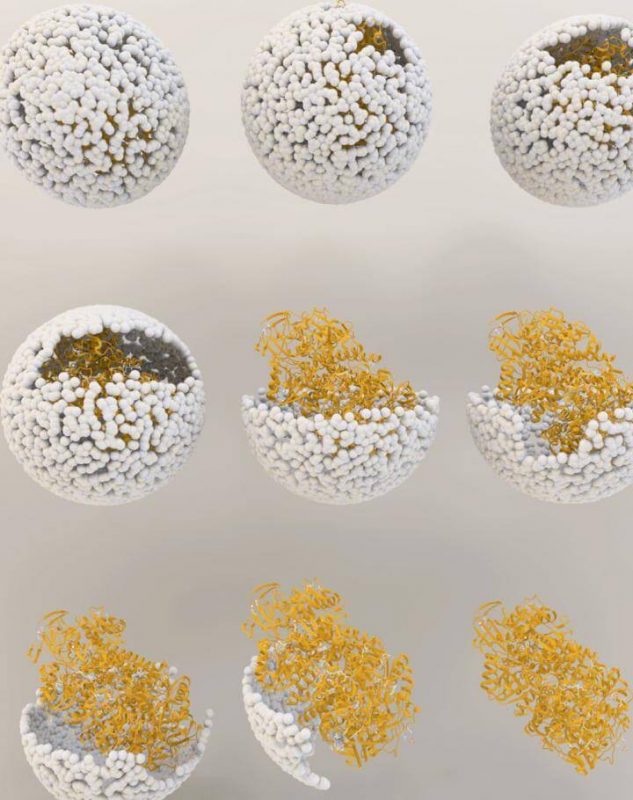
Proces uwalniania się hydrogenaza NiFe ze środka powłoki wirusa. Fot. Indiana University
Materiał genetyczny, który posłużył do stworzenia enzymu, hydrogenaza, wytwarzany jest przez dwa geny z pospolitej bakterii Escherichia coli, umieszczonej w środku ochronnego kapsydu, korzystając z metod opracowanych wcześniej przez naukowców UI. Oba geny, hyaA i hyaB, są dwoma genami E. coli, które kodują główne podjednostki enzymu hydrogenaza. Kapsyd pochodzi z wirusa bakterii znanego jako bakteriofag P22.
Powstała w rezultacie fuzja hydrogenazy i powłoki wirusa jest nie tylko o wiele wydajniejsza w katalizowaniu produkcji wodoru – jest również prostsza w tworzeniu, wymagając jedynie prostego procesu fermentacji. W porównaniu do innych sposobów wytwarzania ogniw paliwowych, jak korzystanie z platyny do katalizy wodoru, jest tania i nie wpływa w znaczący sposób na środowisko.
“Materiał jest podobny do platyny, z wyjątkiem tego, że jest naprawdę odnawialny, w pełnym tego słowa znaczeniu,” powiedział Douglas. “Nie musimy go wydobywać; można wytworzyć go samodzielnie w pokojowej temperaturze na dużą skalę, korzystając z technologii fermentacji; jest biodegradowalny. To naprawdę zielony proces, który wytwarza wysoce nowoczesny i wydajny materiał.”
Oprócz łamania łańcuchów chemicznych wody do produkcji wodoru, P22-Hyd katalizuje również reakcję w drugą stronę, łącząc ponownie wodór i tlen, aby wytworzyć energię.
Rodzaj hydrogenazy, której używają naukowcy – NiFe (nikiel-żelazo) – jest jednym z zaledwie trzech występujących w naturze, ale jest też najlepiej przystosowany do zadania; w prosty sposób można zintegrować go z biomateriałami, toleruje obecność tlenu, a w swej zmienionej, ochranianej wersji, enzym jest o wiele lepszy od niezmienionego enzymu NiFe, dzięki wyższej odporności na ciepło i chemikalia zawarte w środowisku.
“Nikt nigdy nie wpadł na sposób wytwarzania wystarczająco dużych ilości hydrogenezy, pomimo jej niesamowitego potencjału do produkcji biopaliw,” powiedział Douglas. “Teraz nareszcie mamy metodę stabilizacji i produkcji tego materiału w dużych ilościach – a przy tym w o wiele wydajniejszy sposób.”


You must be logged in to post a comment.