Czy kiedykolwiek zastanawialiście się, czy i jak sprawdzane są szczepionki, które kierowane są do użytku w Polsce? Jak szczelny jest to proces i czy byłby w stanie wyłapać wadliwą partię szczepionek?
[Tekst, który czytasz to gościnny wpis na naszym blogu. Jest długi i zawiera sporo szczegółowych informacji dotyczących tego, jak sprawdzane są szczepionki. Nawet jeśli nie przeczytasz go w całości, zapamiętaj, że tu jest. Gdy następnym razem usłyszysz od kogoś, że szczepionek nie testuje się porządnie, że dzieciom i dorosłym podaje się byle co albo że wszystkich przekupiła big pharma – wróć tu i przeczytaj, jak jest naprawdę. Piotrek]
Zapewne pamiętacie aferę z początku 2018 roku, kiedy to okazało się, że partia zepsutych szczepionek trafiła do pacjentów. Okazało się, że wskutek przerw w dostawach prądu szczepionki były źle przechowywane w niektórych przychodniach i niestety nie wszystkie te placówki przekazały uszkodzone szczepionki do utylizacji. A co dzieje się ze szczepionką, zanim trafi do przychodni? Czy jest badana, sprawdzana pod kątem bezpieczeństwa i kto to robi w Polsce? O tym, jak wygląda ten proces, pisze dla nas Karolina Zioło-Pużuk, doktor nauk humanistycznych, adiunkt na Wydziale Nauk Humanistycznych Uniwersytetu Kardynała Stefana
Wyszyńskiego. Specjalistka w zakresie społecznej odpowiedzialności organizacji oraz komunikacji.
Paczka przybywa do laboratorium
Do Narodowego Instytutu Zdrowia Publicznego – Państwowego Zakładu Higieny (NIZP-PZH) przy ulicy Chocimskiej w Warszawie kilka razy w tygodniu wchodzą kurierzy z małymi pakunkami w rękach. Przy wejściu okazują dokumenty, po czym przechodzą przez dziedziniec i kierują się na trzecie piętro zabytkowego budynku, gdzie, po pokonaniu kolejnej bariery – masywnych drzwi opatrzonych domofonem – zostawiają paczuszkę wraz z towarzyszącym jej grubym plikiem dokumentów w punkcie przyjęcia próbki Laboratorium Zakładu Badania Surowic i Szczepionek.
Dla kuriera to koniec niełatwego zadania dostarczenia pakunku w odpowiednich, ściśle określonych warunkach. Dla jego zawartości – kilku fiolek ze szczepionką i załączonej dokumentacji to dopiero początek drogi poprzez biurka i pokoje laboratoryjne. Tak zaczyna się proces kontroli i bezpieczeństwa szczepionek.
NIZP-PZH od blisko 70 lat jest ośrodkiem państwowej kontroli produktów leczniczych immunologicznych i krwiopochodnych. Zakład Badania Surowic i Szczepionek, gdzie przeprowadza się kontrolę, jest Państwowym Laboratorium Kontroli Produktów Leczniczych (OMCL – Official Medicines Control Laboratory) i należy do Sieci Laboratoriów Kontroli Produktów Leczniczych OMCL (European Network of Official Medicines Control Laboratories– GEON), koordynowanej przez Europejski Dyrektoriat ds. Jakości Leków (EDQM) (https://www.edqm.eu/en/human-biologicals-611.htmlHYPERLINK “https://www.edqm.eu/en/human-biologicals-611.html)”). Laboratorium posiada akredytację Polskiego Centrum Akredytacji (AB509) oraz atestację EDQM (certyfikat EDQM/MJA-100).
„To, co tutaj robimy, to efekt lat doświadczeń, więcej nawet niż stu, gdyż szczepienia mają dwustuletnią historię – mówi dr hab. Ewa Augustynowicz, kierownik Laboratorium Zakładu Badania Surowic i Szczepionek. – Wiele błędów, które w początkach szczepień musiały zostać naprawione, i procedur, które wymagały udoskonalenia, złożyło się na to, jak dziś kontroluje się szczepionki. Wszystko, co się tu dzieje, jest dowodem na prawdziwość twierdzenia , iż szczepionki są najlepiej kontrolowanymi preparatami leczniczymi”- dodaje.
Dokumentacja musi się zgadzać
Pierwszą osobą, do której docierają próbki w laboratorium, jest Urszula Czajka, kierownik Pracowni Ewidencji oraz Kontroli Jakości Laboratorium Zakładu Badania Surowic i Szczepionek. W procesie przyjęcia próbki do badań sprawdzeniu podlegają m.in. nazwa, opakowanie, numer seryjny szczepionki, oznakowania na opakowaniu zewnętrznym i bezpośrednim. Oceniana jest zgodność danych dotyczących próbki z dostarczoną dokumentacją. Weryfikowane są warunki transportu. Dowodem zachowania łańcucha chłodniczego w czasie transportu (temperatura w zakresie 2-8 stopni Celsjusza) jest wydruk z urządzenia monitorującego temperaturę paczki:
„Liczba dostarczanych do nas próbek wynika z badań, jakie jesteśmy zobligowani wykonać dla danej szczepionki – mówi Urszula Czajka. – Wachlarz wykonywanych badań w naszym Laboratorium jest szeroki i obejmuje testy biologiczne, biochemiczne, mikrobiologiczne, serologiczne oraz molekularne”.
Specjalistka dodaje, że zakres badań określają instytucje rejestrujące i odpowiedzialne za bezpieczeństwo szczepień, czyli Europejska Agencja Leków (EMA), Europejski Dyrektoriat ds. Kontroli Leków, Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych” oraz Główny Inspektorat Farmaceutyczny. Ważnymi dla jakości kontroli szczepień dokumentami są również: Rozporządzenie Ministra Zdrowia z dnia 10 kwietnia 2013 r. w sprawie kontroli seryjnej wstępnej produktów leczniczych oraz surowców wykorzystywanych do sporządzania leków recepturowych lub aptecznych, określające, jakie podmioty mogą prowadzić badania potwierdzające bezpieczeństwo szczepień, oraz Farmakopea Europejska określająca „[…] podstawowe wymagania jakościowe oraz metody badań produktów leczniczych i ich opakowań oraz surowców farmaceutycznych”.
Laboratorium otrzymuje od producenta szczepionkę i musi sprawdzić jej jakość, bezpieczeństwo oraz immunogenność, stąd ważne jest, aby pracownicy laboratorium oraz przedstawiciele producentów szczepionek nie byli ze sobą w relacjach mogących budzić wątpliwości etyczne.
„Przychodząc do pracy w NIZP-PZH, podpisujemy deklarację poświadczającą, że między nami a firmami produkującymi szczepionki nie ma związków, nie tylko zawodowych, ale również rodzinnych, które mogłyby skutkować konfliktem interesów – wyjaśnia Marta Prygiel, kierownik Pracowni Badania Szczepionek. – Dlatego kierowane pod naszym adresem oskarżenia, że wszystko, co robimy, to element spisku z firmami farmaceutycznymi, świadczą o tym, że wysuwają je osoby, które nie wiedzą nic o naszej pracy w NIZP – PZH”.
Błąd się nie prześlizgnie
W laboratorium sprawdzana jest każda seria szczepionek wyprodukowanych w Polsce. Podobnie serie szczepionek wyprodukowanych poza Polską i dopuszczonych do obrotu na terenie naszego kraju, kontrolowane są w analogicznych, niezależnych od wytwórcy ośrodkach znajdujących się w każdym kraju europejskim. Dlatego większość serii szczepionek, wyprodukowanych i skontrolowanych za granicą w laboratoriach posiadających tożsame uprawnienia oraz standardy bezpieczeństwa z NIZP-PZH, jest zwalnianych z obowiązku kontroli na mocy decyzji administracyjnej, w oparciu o badania przeprowadzone w innym laboratorium za granicą. Każda seria produktu zwalnianego tą drogą na rynek polski przechodzi szczegółową weryfikację dokumentacji, do czego obliguje Europejska Administracyjna Procedura Zwalniania Serii.
Razem z dokumentacją, w celach identyfikacyjnych, dostarczane jest opakowanie szczepionki. Następnie zgodnie z umową zawartą między NIZP-PZH a Głównym Inspektoratem Farmaceutycznym losowo kontrolowane są wszystkie szczepionki dostępne na rynku, zarówno te produkowane w Polsce jak i za granicą. Kontrola obejmuje również sytuacje, kiedy pielęgniarka lub lekarz podejrzewają jakiekolwiek niezgodności w wyglądzie szczepionki przechowywanej w przychodniach. W tym wypadku kontrola szczepionek znajdujących się w obrocie to już trzeci, po producencie i niezależnym laboratorium z sieci OMCL, poziom sprawdzania jakości, bezpieczeństwa oraz aktywności preparatu.
W przypadku serii szczepionek nadesłanych do NIZP-PZH celem przeprowadzenia kontroli seryjnej wstępnej warunkującej wprowadzenie ich na rynek polski wytwórca zobowiązany jest do przedstawienia protokołu wytwarzania i kontroli danej serii produktu. W protokole tym musi szczegółowo raportować kolejne kroki związane z produkcją serii szczepionki ze wskazaniem metodologii – na poszczególnych etapach produkcji.
Czy ktoś może tu celowo skłamać?
Czy w taką dokumentację może wkraść się błąd? Czy ktoś może celowo skłamać?
„Nawet jeśli ktoś miałby taki zamiar, to jego realizacja byłaby niemożliwa właśnie ze względu na wielostopniową kontrolę procesu produkcji oraz producenta przeprowadzaną przez Inspekcję Farmaceutyczną podczas kilkudniowych audytów – mówi Ewa Augustynowicz. – Producenci przestrzegają również zasad Dobrej Praktyki Wytwarzania opisanej w załączniku do rozporządzenia Ministra Zdrowia z dnia 1 października 2008 roku. I w końcu najważniejsze: każda, nawet najmniejsza nieścisłość, odstępstwo od specyfikacji, błąd czy problem, zostaną wykryte w naszym laboratorium.”
Szczepionki znajdujące się w badaniu są kontrolowane nawet w dni wolne od pracy ze względu na stały monitoring temperatury. Upoważnieni pracownicy sprawdzają, czy temperatura w urządzeniach chłodniczych nie odbiega od deklarowanych zakresów. Jeśli zdarzą się jakiekolwiek odchylenia, to system prześle alarmową informację na telefony komórkowe wyznaczonych pracowników, którzy będą musieli niezwłocznie przyjechać do laboratorium i – interweniować.
Niezmienny standard
W Pracowni Badania Szczepionek przeprowadza się między innymi laboratoryjne badania jakościowe szczepionek w zakresie aktywności, czyli ich mocy. To tu mają miejsce najważniejsze testy, po przeprowadzeniu których będzie można stwierdzić, że szczepionka jest bezpieczna, a jej skład zgodny z tym, co zostało opisane podczas rejestracji preparatu.
Dodatkowo, w Pracowni Badania Preparatów Immunologicznych oznaczana jest tożsamość szczepionek. W kontroli bezpieczeństwa szczepionek oraz ich produkcji niezwykle ważna jest powtarzalność, którą gwarantuje ściśle określony sposób postępowania z wyjściowym materiałem biologicznym (bakterią lub wirusem) na bazie którego przygotowywane są szczepionki.
Wszystkie szczepionki są produkowane w systemie serii siewnych, tzn. że kolejne serie szczepionki produkowane są z puli macierzystych serii szczepów bakterii oraz wirusów przechowywanych w ściśle kontrolowanych warunkach. System ten podaje liczbę możliwych pasaży [czyli kolejnych posiewów], co zapewnia niezmienność substancji czynnej szczepionki. Macierzyste serie siewne wirusa lub bakterii opisywane są szczegółowo podczas badań eksperymentalnych nad szczepionką. Z macierzystych serii siewnych szczepów uzyskiwane są robocze serie siewne służące do produkcji kolejnych partii szczepionek. Producent w dokumentach dostarczanych do kontroli podaje datę przygotowania serii siewnej oraz jej dokładne badania.
fot. U.S. Air Force photo/Senior Airman Vernon Young
Za przykład może posłużyć szczepionka przeciw gruźlicy zawierająca żywy prątek bydlęcy podobny do bakterii wywołującej gruźlicę u ludzi. Został on zmieniony odpowiednio w taki sposób, żeby nie wywoływać stanu chorobowego przy jednoczesnej stymulacji wytworzenia odporności. Przeciwgruźlicza szczepionka BCG stosowana jest od 1921 roku, zaś podszczep bakterii, z którego produkowane są polskie szczepionki, używany jest od 1955 roku.
„Podszczep wykorzystywany w Polsce nosi nazwę Moreau. Charakteryzuje go dużo niższa reaktogenność, w porównaniu ze szczepami stosowanymi do produkcji szczepionki przeciwgruźliczej w innych krajach, a co za tym idzie, mniejsza liczba niepożądanych odczynów, przy zachowanej skuteczności. Spełnia on wszystkie warunki niezbędne do wyprodukowania skutecznej i bezpiecznej szczepionki – mówi Katarzyna Krysztopa-Grzybowska zajmująca się badaniami tożsamości szczepionki BCG. – Aby mieć całkowitą pewność, że mamy do czynienia z tym, a nie innym podszczepem, prowadzone są u nas badania molekularne. Pozwalają one bez wątpliwości określić tożsamość, czyli identyfikację podszczepu. Pomyłki co do podszczepu się nie zdarzają, ale wykonujemy badania, gdyż musimy mieć całkowitą pewność. W badaniu nad bezpieczeństwem szczepionek nie ma miejsca na niedociągnięcia”.
Laboratorium nie z serialu
Paulina Górska, kierownik Pracowni Immunochemii, oprowadzanie po swojej pracowni zaczyna od pokazania imponującej liczby segregatorów szczelnie wypełnionych kartkami zapisanymi drobnym maczkiem, gdzieniegdzie – uzupełnionym tabelami i wykresami. To nie wszystko. Podobne opasłe księgi leżą przy każdym urządzeniu w laboratorium. Osobie odwiedzającej może się wydawać, że spaceruje nie po laboratorium, ale po miejscu pracy skrupulatnego skryby. W niczym miejsce to nie przypomina również laboratorium warszawskich Filtrów, w którym pracowała żona serialowego Czterdziestolatka – nikt tu nie plotkuje nad mikroskopem i nie pije herbaty podczas badania. Część biurowa i socjalna jest wyraźnie odseparowana od części laboratoryjnej.
„Papierologia” jest dowodem na rzetelność badań prowadzonych w systemie zarządzania jakością zgodnie z normą ISO 17025. Wymagana jest ona także przez wewnętrzne i zewnętrzne kontrole krajowe i zagraniczne oraz Farmakopeę Europejską, opisującą jakościowe oraz ilościowe badania, jakim podlegają produkty lecznicze. Analizy wykonywane są w klimatyzowanym pomieszczeniu, w którym panuje określona temperatura i wilgotność.
„Każda próbka, która do nas dociera, jest rejestrowana i badana zgodnie z ustalonym schematem. Sprawdzane są właściwości fizykochemiczne produktu, zawartość substancji pomocniczych, czy też zanieczyszczenia, do których może potencjalnie dojść podczas produkcji, co, jak wynika z mojego już ponad dziesięcioletniego doświadczenia, praktycznie się nie zdarza – opisuje główne założenia pracy swojej i innych osób zatrudnionych w Pracowni Paulina Górska – Wiem, że rodzice często pytają właśnie o substancje pomocnicze w szczepionkach, przede wszystkim formaldehyd, którego śladowe ilości dopuszczalne są w produkcie. Są to wartości bezpieczne zarówno dla dziecka, jak i dorosłego. W życiu codziennym mamy większą ekspozycję na formaldehyd, który znajduje się na przykład w kosmetykach czy też środkach czystości”.
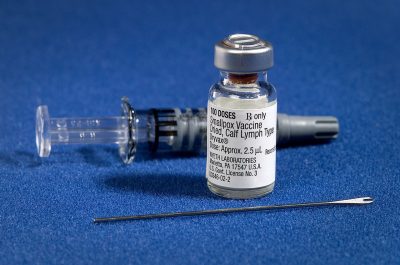
Fot. James Gathany/CDC
Badania wykonują jedynie pracownicy przeszkoleni i upoważnieni do przeprowadzania danej procedury, zaś szkolenia do wykonywania wszystkich metod wykorzystywanych w Laboratorium trwają średnio dwa lata. Wyposażenie podlega regularnej kalibracji, sprawdzaniu okresowemu i bieżącemu, jest legalizowane i sprawdzane według ustalonych procedur. Każde użycie sprzętu jest rejestrowane w przypisanej mu książce aparatury. Nawet ocena wyglądu, wydawałoby się, zwyczajne oglądanie fiolki ze szczepionką jest działaniem opisanym osobną procedurą, w której podana jest dokładna ilość luksów lampy oświetlającej miejsce, gdzie odbywa się to badanie okiem nieuzbrojonym. Co więcej, jedynie osoby upoważnione i przeszkolone mogą odpowiednio ocenić stan próbki.
Wyniki badania preparatu potwierdzane są każdorazowo próbą kontrolną, wpisywane w odpowiednie formularze, a ewentualne nieprawidłowości od przyjętych norm zostałyby wykryte na podstawie kart sterowania jakością. Co więcej, odchylenia nie mieszczące się w granicach normy określonej w specyfikacji muszą być sprawdzone, zaś powody ich powstania dokładnie prześledzone. W razie wystąpienia konieczności, podejmowane są działania korygujące lub naprawcze.
Czasem czuję złość
Pracownicy Zakładu Badania Surowic i Szczepionek nie żyją w laboratoryjnej bańce i doskonale wiedzą, jakie zarzuty wysuwane są przez przeciwników szczepień. Kwestia bezpieczeństwa szczepień nie jest dla nich teoretycznym sporem prowadzonym na forum internetowym, ale ośmiogodzinną codziennością, żmudną pracą, którą tak łatwo przeciwnikom szczepień jest kwestionować.
„Czujemy ciężar odpowiedzialności, jaki ciąży na nas ze względu na kontrolę jakości i bezpieczeństwa szczepionek – mówi Paulina Górska – Potrzebne jest również zaangażowanie. Jeśli ktoś nie może uwierzyć w etykę pracownika laboratorium, to powinny go uspokoić wielostopniowe kontrole, którym podlega nasza praca.”
Dla tak zwanego „świętego spokoju” pracownicy laboratorium mogliby nie reagować na hasła, że szczepienia rzekomo zabijają ludzi, ale w ich obliczu nie potrafią zachować stoickiego spokoju. Nie mogą słuchać pseudonaukowych bzdur chętnie powtarzanych przez osoby nie mające nic wspólnego z badaniami naukowymi nad bezpieczeństwem szczepień. Większość ludzi głoszących te teorie nie ma pojęcia, jak naprawdę wygląda praca w laboratorium NIZP-PZH. Dlatego nie zawsze udaje się trzymać emocje na wodzy:
„Coraz częściej czuję irytację. Odnosi się ona do niewiedzy i ignorancji osób, które tak beztrosko kwestionują moją pracę nie wiedząc, na czym ona polega – mówi Marta Prygiel kierownik Pracowni Badania Szczepionek – Jadąc do pracy, w autobusie, słyszę dyskusje o szczepieniach. Włos się jeży na głowie, jakie herezje ludzie mówią! Najgorzej, kiedy chcą odraczać szczepienia, czekać, aż dziecko będzie starsze. Przecież właśnie dane szczepienie jest w określonym miejscu w kalendarzu szczepień, żeby chronić te najmłodsze, najbardziej narażone na ciężki przebieg choroby i powikłania. Mogę się podpisać pod zdaniem, że szczepionki są szczegółowo kontrolowane. Co więcej, ja się codziennie, pod tym podpisuję. I szczepię moje dzieci”.
Pod bezpieczeństwem szczepień osobisty podpis bez wahania składają wszyscy pracownicy Zakładu Badania Surowic i Szczepionek Narodowego Instytutu Zdrowia Publicznego – Państwowego Zakładu Higieny.

You must be logged in to post a comment.