Dlaczego – pomimo ogromnego postępu metod badawczych – wciąż prowadzi się badania na zwierzętach? Czy to rzeczywiście konieczne? Jakim ograniczeniom podlega eksperymentator i czy faktycznie jest kontrolowany? O badaniach na zwierzętach pisze dla Crazy Nauki Ewa Biela, doktor nauk biologicznych z doświadczeniem zawodowym zdobytym na Uniwersytecie Jagiellońskim, Purdue University (USA) i na Uniwersytecie w Namur (Belgia).
Badania na zwierzętach rodzą duże wątpliwości natury etycznej i budzą bardzo silne emocje. To zupełnie naturalne, gdyż z jednej strony mamy dyskomfort, cierpienie i przedwczesną śmierć zwierząt, z drugiej poszerzenie wiedzy, ale też nowe terapie i zmniejszenie cierpienia chorych – tak ludzi jak i zwierząt. I jak bardzo kompromisowo nie chcielibyśmy podejść do tego tematu, zawsze ktoś będzie pokrzywdzony.
Nowoczesna terapia ratująca życie tysiącom ludzi to niewielka pociecha dla szczura, na którym eksperymentowano by ją opracować. Jednocześnie zaniechanie eksperymentów oznaczałoby kompletny zastój w rozwijaniu nowych zabiegów medycznych i terapii, które pomogą w przyszłości nawet milionom ludzi i zwierząt.
Modele zwierzęce działają
Podejmowane są liczne starania, by zastąpić tak zwane modele zwierzęce innymi modelami lub przynajmniej wykorzystywać zwierzęta, które czują mniej bólu czy emocji. Rozwijają się symulacje komputerowe czy badania in vitro (czyli prowadzone poza organizmami zwierzęcymi). Kiedyś “in vitro” oznaczało jedynie luźno rosnące komórki, przykryte cieniutką warstewką pożywki, później wprowadzono kohodowle i multihodowle – czyli mieszaniny różnych typów komórek, a także trójwymiarowe zlepki komórek – sferoidy[1] , dla lepszego badania interakcji w przestrzeni. Obecnie rozwijane są techniki wytwarzania organoidów[2] , uproszczonych i zminiaturyzowanych „organów” sztucznie hodowanych w laboratorium, które pozwalają symulować wiele procesów zachodzących w organizmach żywych.
Badania in ovo (w jajku kurzym) pozwalają na prowadzenie eksperymentów, w których istotna jest obecność naczyń krwionośnych i transport substancji we krwi.
To imponujące osiągnięcia i wspaniale, że można z nich korzystać. Ale jak każdy uproszczony model, nie są one doskonałe. Organizm jest dużo bardziej złożoną maszynerią i niektórych z zachodzących w nim procesów po prostu nie jesteśmy w stanie wymodelować z wystarczającą dokładnością, a pewne elementy nie dadzą się wymodelować w ogóle. Dlatego wykorzystanie zwierząt laboratoryjnych w takich sytuacjach jest jedyną szansą dla dalszego rozwoju biologii czy medycyny.
Czasem ktoś argumentuje, że mysz to nie to samo co człowiek i takie badanie zrobione na myszach nie ma żadnej wartości. To nieprawda. Pomiędzy myszą a człowiekiem różnica jest ogromna, ale u myszy i człowieka 85% genów kodujących białka jest identycznych. Mysz (ale też szczur, chomik, a nawet ryba) jest wciąż modelem o wiele doskonalszym niż wszystko, co możemy zrobić w szalce z komórkami. Hodowla komórek nowotworowych na szalce może przydać się do oceny, jak dany preparat radzi sobie z izolowanymi komórkami, czy też w jaki sposób na nie działa, ale nie powie nic o interakcji tegoż nowotworu z układem immunologicznym, o jego ukrwieniu, o tym, jak przyjmie on lek, jak wpłynie to na tworzenie przerzutów czy same przerzuty, a jak na tempo wzrostu pierwotnego guza.
Bez zwierząt nie ma postępu medycyny
Sprawa jest prosta. Albo będziemy prowadzić eksperymenty na zwierzętach, albo nie będzie nowych leków i terapii, nie będzie postępu w technikach diagnostycznych, chirurgii, czy nawet stomatologii.
Aby lepiej zobrazować, jak istotne są te eksperymenty, podam kilka przykładów.
Dzięki badaniom na świniach mamy możliwość wykonania skanów tomografii komputerowej i zyskaliśmy nowe metody leczenia oparzeń (w tym przeszczepy „sztucznej skóry”). I nie piszę tu o bolesnym przecież oparzeniu drugiego stopnia, ale o oparzeniach, w wyniku których skóra przestaje istnieć, dając pole zakażeniom, ale i umożliwiając ucieczkę wody i osocza krwi z organizmu.
Należy przecież pamiętać, że oparzenie dużej powierzchni skóry jest śmiertelne. Wg WHO rocznie 265000 osób umiera z powodu oparzeń wywołanych przez ogień . Do tego dochodzą oparzenia chemiczne, jak i te wywołane przez gorące płyny. W Polsce co roku około 12000 osób wymaga z ich powodu hospitalizacji, a około 600 nie udaje się uratować. Znaczna część pacjentów na oddziałach oparzeniowych to dzieci. Opatrunki ze „sztucznej skóry” stosuje się także przy leczeniu trudno gojących się ran i owrzodzeń.
Dzięki eksperymentom na świniach opracowano również wiele zabiegów chirurgicznych, których inaczej po prostu nikt nie umiałby wykonać.
Świnki morskie (czyli kawie domowe) to jedyne poza człowiekiem ssaki, które nie są zdolne do syntezy witaminy C. Ich udział w badaniach nad szkorbutem i nieprawidłową polimeryzacją kolagenu okazał się bezcenny. A problemy z syntezą i polimeryzacja kolagenu to nie tylko szkorbut, ale też różnego rodzaju kolagenozy czy też wrodzona łamliwość kości, czasem tak silna, że nawet naturalny poród skutkuje licznymi złamaniami kości noworodka.
Kraby wykorzystuje się do badań nad koordynacją funkcji ruchowych z racji tego, że liczba ich neuronów ruchowych jest bardzo niewielka.
Zwierzęta naczelne podlegają wyjątkowo ścisłej ochronie, ale niekiedy i one wykorzystywane są w eksperymentach. Na rezusach prowadzi się badania z indukowanym parkinsonizmem, na przykład polegające na głębokiej stymulacji mózgu. A pod tym linkiem można zobaczyć efekty takich badań.
Ogromne ucho wewnętrzne szynszyli pozwala na badanie terapii zapalenia ucha, która to infekcja wcale nie jest taka banalna, jak się wielu wydaje.
Dziś nikt nie wyobraża sobie diagnostyki bez zaawansowanych technik obrazowania. Diagnostyka zaawansowania choroby nowotworowej bez badania PET, pozwalającego na zlokalizowanie przerzutów, nie byłaby możliwa. Przeszczep serca? Bez doświadczeń na zwierzętach on również nie byłby możliwy, podobnie jak badanie nowych antybiotyków (a że stare przestają działać, to wiemy chyba wszyscy), opracowanie nowych szczepionek czy mechanizmu transmisji wirusów, uzyskanie antytoksyn… Także dzięki badaniom na zwierzętach już dziś mamy niewielkie możliwości regeneracji uszkodzeń kręgosłupa.
Ocena etyczna
Lista powodów, dla których wciąż prowadzimy eksperymenty na zwierzętach, jest bardzo długa. Jednak w każdym konkretnym przypadku konieczne jest dokładne rozważenie, czy dany eksperyment ma szansę powodzenia, czy może przynieść odpowiedzi na postawione pytania i czy w związku z tym może być etycznie usprawiedliwiony.
W 2018 roku w Polsce wykorzystano w doświadczeniach ponad 153 tys. zwierząt, wśród których niemal trzy czwarte to myszy i szczury. Te liczby wydają się ogromne, ale okazują się niewielkie przy liczbie np. kurczaków hodowanych i ubijanych na mięso – według danych GUS w 2015 roku w Polsce było ich prawie 997,5 mln.
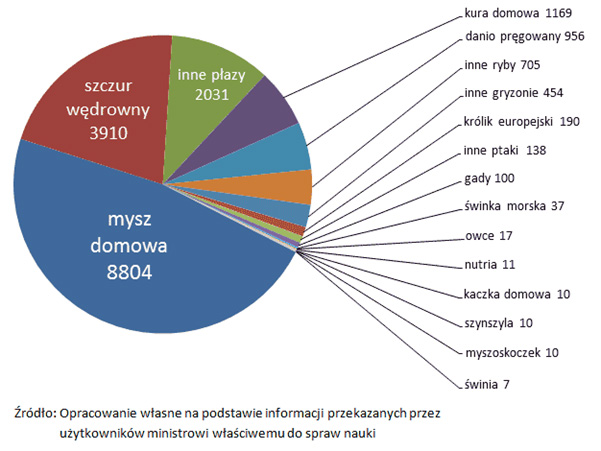
Regulacje dotyczące badań na zwierzętach
Początki obecnemu europejskiemu prawu i regulacjom dały ruchy antywiwisekcjonistów w Anglii (ok. 1870 roku). Tak, były czasy, kiedy uważano, że zwierzęta nie czują, a ich walkę o życie i skowyt przy sekcji na żywo interpretowano jako proste odruchy mające zapewnić im przetrwanie. Obecnie wiemy, że zwierzęta czują ból, strach, potrafią przeżywać żałobę po stracie partnera czy opiekuna, a emocjonalnie mogą być tak rozwinięte jak kilkuletnie ludzkie dzieci.
Nowe prawo wprowadzono w Anglii w 1876 roku, ale powstanie europejskiej konwencji i sformułowanie wytycznych, na podstawie których pozostałe kraje europejskie opracowały własne, niemal identyczne przepisy, zajęło dodatkowe 100 lat.
Pierwsza i najważniejsza zasada w doświadczeniach na zwierzętach to 3R:
- Replace (zamień): Zgodnie z ustawą z 2015 roku oznacza to „Wykonywanie doświadczeń tylko w przypadku, gdy nie można zastosować alternatywnych metod badawczych”.
- Reduce (zmniejsz): zgodnie ze wspomnianą wyżej ustawą oznacza to „ograniczenie liczby zwierząt wykorzystywanych w procedurze do poziomu niezbędnego”, oraz
- Refine (udoskonal) co wg ustawy z 2015 roku oznacza „Utrzymywanie zwierząt w warunkach środowiskowych odpowiednich do ich gatunku oraz zastosowanie metod ograniczających do minimum albo eliminujących ból i dystres”.
W praktyce przekłada się to na zmniejszenie liczby zwierząt, zmniejszenie liczby procedur wykonywanych na tych zwierzętach i ich uciążliwości (eksperyment na zwierzętach ma uzasadnienie tylko wtedy, kiedy inne metody zostaną wyczerpane, a wnioski z ich zastosowania pozwalają przypuszczać, że doświadczenie da wynik, który wniesie coś nowego czy to w terapii, diagnostyce czy też pozwoli uzyskać nowe informacje na temat procesów zachodzących w organizmach żywych).
Tam, gdzie jest to możliwe, wykonuje się symulacje i doświadczenia in vitro. Istnieją bazy danych zawierające opisy alternatywnych metod badawczych, które planujący badanie jest zobowiązany przeszukać, zanim w ogóle zacznie planować eksperyment z udziałem zwierząt.
- ALTWEB, Alternatives to Animal Experimentation, is the official publication of the Johns Hopkins Center for Alternatives to Animal Testing (CAAT);
- ALTBIB, Resources for Alternatives to the Use of Live Vertebrates in Biomedical Research and Testing;
- AnimAlt ZEBET, Centre for Documentation and Evaluation of Alternatives to Animal Experiments (AnimAlt-ZEBET);
- Invitroderm, alternatives to skin irritation tests on animals;
- ECVAM unijne centrum walidacji alternatyw i metod niezwierzęcych, działa w Europie.
Tam, gdzie trzeba wykorzystać zwierzęta, minimalizuje się liczbę procedur, a te niezbędne zamienia się na mniej inwazyjne (na przykład podaje się lek podskórnie zamiast dootrzewnowo, stosuje się nieinwazyjne obrazowanie np. stanu narządów wewnętrznych zamiast uśmiercania kolejnych zwierząt w kolejnych punktach czasowych i oceny stanu organów podczas sekcji). Używany jest najlepszy możliwy sprzęt, stosowane są środki przeciwbólowe, a warunki bytowania zwierząt są optymalizowane, by zaoszczędzić im stresu, bólu i każdej możliwej formy dyskomfortu. Niedopuszczalne jest wykonywanie danej procedury, jeżeli wiąże się ona z dotkliwym bólem, cierpieniem lub dystresem (czyli reakcją organizmu na zagrożenie, utrudnienie lub niemożność realizacji ważnych celów i zadań), który może mieć długotrwały charakter i nie można go załagodzić.
Zanim dojdzie do badań z udziałem zwierząt
Dla prostszego wyjaśnienia użyję przykładu: w badaniach in vitro okazuje się, że dany związek chemiczny wbudowuje się w DNA dzielących się komórek i uszkadza je, prowadząc do śmierci tych komórek, pozostając praktycznie bez wpływu na komórki niedzielące się. Załóżmy, że cząsteczka tego związku jest niewielka i ma takie właściwości, że zgodnie z modelami teoretycznymi powinna przenikać przez barierę krew-mózg i być może mogłaby mieć zastosowanie w leczeniu nowotworów mózgu.
Nikt nie weźmie probówki z owym związkiem i nie wstrzyknie go myszom bez wcześniejszych dokładnych badań. Najpierw trzeba sprawdzić, czy nikt nie wpadł na taki sam pomysł wcześniej i czy nie ma już opublikowanych wyników podobnego eksperymentu.
Tu kolejna ważna rzecz: w przypadku pracy ze zwierzętami laboratoryjnymi cenne są również publikacje naukowe opisujące nieudane eksperymenty. Normalnie wartość takich prac jest mała i nikt nie zawraca sobie głowy publikowaniem czegoś, co nie działa w eksperymentach na liniach komórkowych (a bardzo szkoda), ale w przypadku eksperymentów z udziałem zwierząt takie prace mają znacznie większą wagę. Chodzi o to, by inny zespół badawczy, który miał ten sam pomysł, nie prowadził bezsensownego eksperymentu i nie narażał zwierząt na niepotrzebne cierpienie. Takie przynajmniej jest założenie, i takie są wytyczne, choć przyznam, że liczba takich publikacji wciąż jest zbyt mała.
Po przeszukaniu baz danych i dostępnych publikacji przychodzi czas na symulacje komputerowe i badania in vitro. W badaniach na komórkach bada się, w jakim stopniu ów związek jest toksyczny, jaki procent komórek nowotworowych zabija i w jaki sposób, oraz na jaki rodzaj nowotworu będzie działał najlepiej. Trzeba też sprawdzić, jakie ów związek chemiczny wywołuje zmiany w komórkach powstałych z podziałów tych, którym udało się zsyntetyzować swoje DNA i podzielić się pomimo jego obecności, oraz ustalić, w jakiej dawce powinien być podany w eksperymencie in vivo, czyli na żywym organizmie (pamiętajmy, toksyczność jest zależna od dawki). Pula dostępnych tu analiz jest bardzo duża.
Jeśli na tym etapie coś idzie nie tak (na przykład uszkodzenia w komórkach są nieznaczne i skuteczność preparatu będzie niewielka, a zwiększenie dawki powoduje toksyczność innego rodzaju, niż ta, której oczekujemy), formuła ląduje w koszu i nikt nie zawraca sobie nią głowy.
Kiedy można uzyskać zgodę na badania na zwierzętach?
Dopiero później, mając wyniki – o ile są one korzystne – można wystąpić o zgodę komisji bioetycznej na przeprowadzenie badań na zwierzętach.
Zgoda komisji bioetycznej jest niezbędna i bez niej nie wolno nawet zakupić zwierząt do eksperymentu. Wniosek musi zawierać szczegółowe wyjaśnienie, dlaczego dany eksperyment musi być przeprowadzony na zwierzętach i dlaczego nie da się zastąpić użycia zwierząt innym modelem. Liczba zwierząt biorących udział w eksperymencie musi być tak mała, jak to możliwe, ale na tyle duża, by była szansa na uzyskanie jednoznacznego (istotnego statystycznie) wyniku. Najgorszym, co można zrobić, to przeprowadzić eksperyment i uzyskać nic nie znaczący wynik, bo wtedy cierpienie i często śmierć zwierząt poszłyby na marne.
Niekiedy możliwa jest opcja „współdzielenia zwierząt”. Na przykład ktoś, kto potrzebuje jedynie zwierzęcych tkanek, pobranych po śmierci, może skorzystać z tkanek zwierząt z puli kontrolnej służących do innego eksperymentu. Ogromnym bonusem jest to, że na pobranie tkanek po uśmierceniu zwierzęcia nie jest wymagana zgoda komisji bioetycznej, a to ułatwienie dla eksperymentatora. Sama wykonałam w ten sposób obrazowanie wciąż żywych (w sensie aktywności metabolicznej) tkanek zwierzęcych.
A co z trzecim R (pamiętacie? “Replace Reduce Refine”)? Już na etapie wniosku do komisji bioetycznej trzeba dokładnie opisać, w jakich warunkach zwierzęta będą przetrzymywane. Są precyzyjne regulacje dotyczące rozmiaru klatki, tego, co w klatce ma się znaleźć, by zapewnić zwierzęciu komfort. Regulowane jest nie tylko oświetlenie zwierzętarni, ale też liczba cykli wymiany powietrza, temperatura i wilgotność. Trzeba zaplanować wszystkie procedury, ograniczając te inwazyjne, zapewniając znieczulenie i ewentualne środki przeciwbólowe, jeśli procedura może wiązać się z bólem.
Zwierzęta w eksperymencie są monitorowane – ważone, obserwowane pod kątem równości i tempa oddechu, oznak bólu – znacznie częściej i dokładniej niż wiele zwierząt domowych (przykładowe tablice skali bólu u myszy, szczurów i królików).
W placówce badawczej musi być zatrudniony weterynarz, a osoby, które wykonują eksperymenty, muszą być przeszkolone i mieć stosowne doświadczenie. Kontrolujący stan zwierząt i sprzątający klatki technicy również muszą przejść odpowiednie przeszkolenie. Nikt, kto nie ma odpowiedniego wykształcenia i nie przeszedł szkolenia, nie ma nawet dostępu w pobliże zwierząt.
Zanim zacznie się eksperyment, zwierzęta oswaja się nie tylko ze sobą, ale i ze sposobami unieruchomienia (na przykład na potrzebę podania zastrzyku), by zmniejszyć stres w czasie tej procedury. W przypadku psów zaspokaja się ich potrzeby socjalne – również potrzebę kontaktu z człowiekiem.
W Polsce początkujący badacz (będący już po kursach i egzaminie) przez minimum rok wykonuje wszystkie procedury tylko pod nadzorem. Zaś ci, który planują doświadczenia (co wcale nie jest prostym zadaniem), muszą mieć za sobą co najmniej cztery lata wykonywania procedur.
Komisja bioetyczna
W komisji bioetycznej zasiadają specjaliści z wielu dziedzin: weterynarze, etycy, specjaliści od statystyki, a także przedstawiciele organizacji społecznych, których celem jest ochrona zwierząt.
Badania zaczyna się od wstępnych prób na małej ilości zwierząt. Chodzi o to, by uniknąć sytuacji, gdzie duże grupy poddawane są niesprawdzonym procedurom. Jeśli na którymś etapie badań wstępnych ujawni się problem z badanym potencjalnym lekiem czy procedurą badawczą, procedura ta jest modyfikowana lub badanie jest przerywane – dlatego, że po pierwsze, nie ma etycznego usprawiedliwienia dla jego kontynuowania, po drugie, nikt nie będzie spędzał godzin pracy i wydawał mnóstwa pieniędzy na eksperyment, z którego nic nie wyniknie. Ten zwyczajny, zimny pragmatyzm działa na korzyść zwierząt, gdyż przekłada się również na ich traktowanie.
Gdyby ktoś na przykład chciał zaoszczędzić i zaniedbywał zwierzęta, wyniki jego badań staną się niewiarygodne. Bo jak badać skuteczność leku na astmę, jeśli zwierzę cierpi z powodu poważnej infekcji? Jak badać lek na żołądek, kiedy niekorzystne warunki w klatce wywołują dodatkowo frustrację lub powodują dystres?
Tyle teoria, a jak wygląda to w praktyce?
Prawie wszystkie jednostki badawcze działają zgodnie z wytycznymi. W placówkach badawczych zdarzają się niezapowiedziane kontrole, a w przypadku poważnych nieprawidłowości jednostka badawcza traci prawo do pracy ze zwierzętami.
Czasem świat obiegnie wstrząsająca relacja, jak ta z Laboratorium Farmakologii i Toksykologii (LPT) w Niemczech, gdzie pomimo kontroli nie wykryto skali nieprawidłowości (dlatego, że akurat w czasie kontroli nie prowadzono tam eksperymentów), a prawdę o tym, jak wyglądają badania, ujawnili wolontariusze organizacji walczących o prawa zwierząt. To dowodzi, że jak w każdej aktywności w naszym życiu, kontrole nie zawsze są skuteczne i należy prowadzić je częściej.
Na szczęście takie sytuacje to w Europie rzadkość. Inaczej sprawa ma się z krajami takimi jak Chiny czy na Bliskim Wschodzie, gdzie religia stawia zwierzęta na równi z przedmiotami. Brak jakichkolwiek regulacji, brak jakiejkolwiek ochrony zwierząt laboratoryjnych, brak środków znieczulenia, brak limitów tego, na jak dużo i jak bolesnych procedur można zwierzę narazić. Nie będę przytaczała tego, co sama przeczytałam i usłyszałam, gdyż niektóre relacje były naprawdę wstrząsające. Jako przykład podam tylko wypowiedź: „Wiesz, my chcielibyśmy móc podać tym zwierzętom środki przeciwbólowe, ograniczyć ich cierpienia, ale zwyczajnie ich nie mamy. Projekt nie przewiduje takiego zapotrzebowania i nic nie możemy zrobić”. Świadomość, że tak jest, jest bardzo trudna do zniesienia.
Na razie nie ma możliwości rezygnacji z badań z udziałem zwierząt
Jednak przepisy i kontrole nie są jedynym czynnikiem, który powoduje, że zwierzęta laboratoryjne w większości przypadków dostają najlepszą możliwą opiekę. Naukowcy wykonujący eksperymenty z ich udziałem to też ludzie. W dodatku ludzie posiadający wiedzę o tym, że zwierzę czuje, że się boi. Wielu badaczy ma opór przed wykonywaniem doświadczeń z udziałem zwierząt i jedynie świadomość, jak wiele może się zmienić w medycynie (ale i weterynarii!), przekonuje ich do wykonywania eksperymentów z udziałem zwierząt laboratoryjnych. Takie badania powinni (i w ogromnej większości robią) ludzie świadomi etycznych dylematów i obdarzeni empatią.
Podsumowując: dążymy do tego, by maksymalnie zmniejszyć liczbę zwierząt wykorzystywanych w badaniach naukowych, rozwijamy niezwierzęce modele badawcze, jednak na chwilę obecną nie mamy możliwości całkowitej rezygnacji z tego rodzaju eksperymentów. Kontrolujemy warunki, w jakich bytują zwierzęta, eksperymenty są oceniane zarówno przed, w trakcie jak i po ich realizacji.
Z pewnością wciąż możliwa jest rezygnacja z niektórych eksperymentów, dalsza poprawa kontroli akceptacji wniosków, a także kontrola samych jednostek prowadzących badania i toczących się eksperymentów. Obecnie nacisk na publikowanie wyników nieudanych eksperymentów jest zbyt mały, choć istnieją specjalne bazy danych, gdzie można zamieszczać ich opisy. Odpowiednie odgórne regulacje mogłyby poprawić sytuację. Wciąż zbyt mało popularne jest także współdzielenie zwierząt, kiedy jeden z badaczy potrzebuje jedynie izolowanych tkanek.
Na koniec dodam, że badania nastawienia ludzi niebędących naukowcami wskazują jednoznacznie, że ci, którzy mieli okazję dowiedzieć się więcej o tym, jak prowadzone są badania z udziałem zwierząt, obejrzeć filmy z nagranymi procedurami i zobaczyć, jak żyją zwierzęta wykorzystywane w eksperymentach, są tym eksperymentom mniej przeciwni. Również z tego powodu razem z wnioskiem dla komisji bioetycznej składa się uproszczone, zrozumiale dla szerszego ogółu „streszczenie nietechniczne” – które ma być napisane zrozumiałym językiem i w zwięzły sposób określać cel i zasadność badań związanych z konkretnym wnioskiem.
[1] Chin Siang Ong et al., In vivo therapeutic application of cell, spheroids, Biotechnology Advances 36, 494-505 (2018)
[2] Hans Clevers, Modeling Development and Disease with Organoids. Cell 165, 1586–1597 (2016)

You must be logged in to post a comment.